Nutriční léčba a riziko podvýživy u seniorů s chronickým onemocněním ledvin – naše dlouholeté zkušenosti a algoritmus výživové péče dle ESPEN a ERN-ERA
Nutritional management and risk of malnutrition in seniors with chronic kidney disease – our long-term experience and algorithm by ESPEN and ERN-ERA
Increased life expectancy includes a sharp increase in the prevalence of chronic kidney disease (CKD) and of impaired nutritional status with malnutrition-protein-energy wasting (PEW) that portends worse clinical outcomes, including reduced survival. In seniors with CKD, a nutritional dilemma occurs when indications from geriatric nutritional guidelines to maintain the protein intake above 1.0 g/kg/day to prevent malnutrition need to be adapted to the indications from nephrology guidelines, to reduce protein intake in order to prevent or slow CKD progression and improve metabolic abnormalities.
These issues were repeatedly addressed by the European Society for Clinical Nutrition and Metabolism (ESPEN) and the European Renal Nutrition group of the European Renal Association (ERN-ERA) and are very important clinical problems in management of conservative treatment in seniors with CKD.
Based on our long-term experience there is a need for careful assessment to identify the presence of malnutrition-protein-energy wasting (PEW) just before reduction of protein intake, regular control of the metabolic and nutritional status and frequently also the use of nutritional supplements such as keto amino acids or renal enteral nutritional products for sipping.
The presence of malnutrition-protein-energy wasting (PEW) suggests the need to avoid or postpone protein restriction, particularly in the presence of stable kidney function and considering the patient’s preferences and quality of life.
Keywords:
chronic kidney disease – seniors – keto amino acids – protein-energy wasting – low-protein diet
Autoři:
Vladimír Teplan 1-5; Ondřej Gojiš 3
Působiště autorů:
Interní a kardiologická klinika Fakultní nemocnice Ostrava a Lékařská fakulta Ostravské univerzity, Ostrava
1; Katedra interních oborů Lékařské fakulty Ostravské univerzity
2; Klinika Ambicare, Praha
3; Subkatedra nefrologie, Institut postgraduálního vzdělávání ve zdravotnictví, Praha
4; Codum s. r. o., Praha
5
Vyšlo v časopise:
Geriatrie a Gerontologie 2026, 15, č. 1: 11-21
Kategorie:
Přehledový článek
doi:
https://doi.org/10.61568/geri/50-6703/20260311/143072
Souhrn
Prodlužující se délka života je spojena s nárůstem prevalence chronického onemocnění ledvin (CKD) a souvisejícím rizikem proteino-energetické malnutrice (PEW), což vede k horším klinickým výsledkům, včetně snížené doby přežití. U seniorů s CKD nastává nutriční dilema, když je třeba podle pokynů geriatrických nutričních doporučení udržet příjem bílkovin nad 1,0 g/kg/den za účelem prevence podvýživy a současně respektovat obecně přijatá nefrologická doporučení se snížením příjmu bílkovin s cílem zpomalení progrese CKD a zlepšení metabolických abnormalit. Tyto otázky byly opakovaně řešeny i Evropskou společností pro klinickou výživu a metabolismus (ESPEN) a Evropskou skupinou pro renální výživu Evropské renální asociace (ERN-ERA) a jsou dlouhodobým problémem klinické praxe konzervativní léčby CKD seniorů.
V souladu s našimi dlouholetými zkušenostmi je třeba individuálního pečlivého posouzení nutričního stavu seniorů ještě před zahájením redukce v příjmu proteinů, pravidelné kontroly nutričního a metabolického stavu a často nezbytné užití nutričních doplňků, jako jsou ketoanaloga esenciálních aminokyselin (KA) a sippingu s produkty v renální formuli. Přítomnost podvýživy, vyčerpávání tělesných bílkovin a energie (PEW) naznačuje potřebu vyhnout se omezení proteinů nebo je odložit, zejména při stabilní funkci ledvin a s ohledem na preference a kvalitu života pacienta.
Klíčová slova:
senioři – chronické onemocnění ledvin – nízkobílkovinná dieta – ketoanaloga esenciálních aminokyselin – proteino-energetická malnutrice
Úvod
Chronické onemocnění ledvin (CKD) je významně častější ve stáří (nejčastěji na podkladě nefrosklerózy a diabetu) a jeho prevalence se odhaduje u seniorů až 30 %. Může současně vést k poruše nutrice, a to až charakteru proteino-energetické malnutrice (PEW). Stárnutí je také nezávisle spojeno s dalším rizikem zhoršení nutričního stavu spojeným s postupnou ztrátou svalové hmoty a její funkce (tj. sarkopenie). Důležité je, že nadváha a obezita, které jsou také běžné u starších dospělých, jsou dalšími rizikovými faktory pro rozvoj a progresi CKD a mohou také přímo podporovat vznik sarkopenie.(1, 2, 3)
Rozvoj podvýživy, stejně jako PEW a sarkopenie, vedou k vyšší morbiditě a mortalitě seniorů, zvyšují riziko jejich křehkosti a snižují kvalitu života ve stáří v jakémkoli klinickém prostředí.(4, 5, 6). Vysoká prevalence podvýživy a sarkopenie ve stáří vedla ke stanovisku Evropské společnosti pro klinickou výživu a metabolismus (ESPEN), která doporučuje, aby starší osoby měly denní příjem bílkovin na úrovni 1–1,2 g/kg, což je více, než jsou doporučené denní dávky v obecné populaci, které jsou v současnosti stanoveny na 0,8 g/kg tělesné hmotnosti za den.(4, 7, 8)
Na druhé straně, obecně přijímaná léčebná strategie pro konzervativní léčbu CKD a jejích komplikací zahrnuje snížení příjmu bílkovin. Směrnice KDOQI z roku 2020 týkající se výživy u CKD doporučují střední, eventuálně až výrazné omezení příjmu bílkovin u pacientů s CKD bez diabetu (0,4–0,6 g/kg/den), s cílem zpomalit progresi onemocnění a korigovat přítomné metabolické poruchy (především hyperazotemii, hyperfosfatemii, hyperkalemii a acidobazickou rovnováhu), ale také udržet adekvátní nutriční stav a odložit začátek dialýzy.(7) Pro pacienty s diabetem se doporučuje mírnější omezení proteinů (0,6–0,8 g/kg/den). Významné je, že doporučení nízkobílkovinných diet bylo nyní rozšířeno na stadium CKD 3 (tj. s odhadovanou glomerulární filtrací – eGFR – mezi 59 a 30 ml/min/1,73 m2, tj. 1–0,5 ml/s) v nepřítomnosti kontraindikací a bez ohledu na věk.(7) Jak geriatrické, tak renální doporučení zdůrazňují potřebu současně dostatečného příjmu energie, aby se předcházelo podvýživě a optimalizovalo se anabolické využití bílkovin a udržování svalové hmoty.(6, 7)
Geriatrické a nefrologické klinické směrnice tedy v současnosti poskytují protichůdná doporučení ohledně denního příjmu bílkovin: aby se předcházelo podvýživě a současně příznivě ovlivnilo metabolický a nutriční stav seniorů s CKD.(9)
Cílem této přehledové práce je shrnutí optimálního postupu dietních opatření, především podávání bílkovin u starší dospělé populace a seniorů, kde se mohou prolínat rizika chronické nefropatie (CKD) a podvýživy.(10, 11)
Nutriční stav a riziko podvýživy u starších dospělých s CKD, PEW a sarkopenií mají překrývající se, ale ne totožné definice.(3) Termín podvýživa je schválen společností klinické výživy pro definici narušeného nutričního stavu neboli podvýživy, termín PEW je častěji používán v nefrologické terminologii a termín sarkopenie se používá při komplikacích specifických pro svalovou hmotu a/nebo její funkci.(4)
Stárnutí je nedílnou součástí životního cyklu a v nejširším smyslu označuje časově podmíněné změny během délky života.(1)Zatímco některé změny nemají zásadní dopady na zdraví, jiné vedou k postupnému zhoršování tělesných funkcí a nakonec k úmrtí.
Chronická onemocnění a jejich komplikace jsou časté ve stáří a obecně zvyšují tyto rizikové faktory, což vede k široké definici podvýživy související s onemocněním, která se může vyskytnout v jakémkoli věku a zvyšuje nutriční riziko, jak je uvedeno v pokynech ESPEN o terminologii klinické výživy.(4)
Senioři s chronickým onemocněním ledvin
S věkem se funkce ledvin tzv. fyziologicky snižuje. Klesá hodnota jak glomerulární filtrace (GF), tak funkcí tubulárních (především koncentrační schopnost ledvin). Odhaduje se, že jinak zdravý senior ve věku 80 let má zhruba poloviční hodnotu GF než člověk ve věku kolem 20. roku. Souběžná onemocnění ledvin ve vyšším věku (diabetes, obezita, nefroskleróza, kardiorenální syndrom apod.) tento rozdíl ještě zvyšují. Tyto nálezy však nejsou přítomny u všech seniorů, existují významné individuální rozdíly.(1) Někteří autoři tvrdí, že eGFR (estimated, tj. odhadovaná GF podle výpočtu) pod 60 ml/min/1,73 m2 (tj. 1 ml/s) ukazuje přítomnost CKD nezávisle na věku, jiní odborníci naznačují, že práh by měl být nižší u starších dospělých. Praktické důsledky jsou relevantní, protože současné směrnice KDOQI pro nutriční management u CKD doporučují nízkobílkovinnou dietu začínající od stadia CKD 3 (eGFR < 60 ml/min/1,73 m2), bez ohledu na věk, aby se odložil začátek dialýzy a předešlo komplikacím souvisejícím s CKD.(7)
Prevalence CKD ve stadiu 3 u starších dospělých může dosáhnout 25–35 %; nastavení mezního bodu pro starší dospělé na eGFR < 45 ml/min/1,73 m2 by snížilo prevalenci na 15–20 %, což by též snížilo indikace ke snížení příjmu bílkovin. Statická definice hodnoty eGFR však neumožňuje rozlišit mezi pacienty se stabilní funkcí ledvin (odhaduje se, že tvoří asi 50 % pacientů s CKD 3) a pacienty s rychlejší progresí.(12) K identifikaci pacientů s rizikem další progrese poškození funkce ledvin, ale také těch, kteří jsou ohroženi komplikacemi, jako jsou kardiovaskulární příhody, jsou nutná longitudinální data o funkci ledvin, protože algoritmy pro přesné prediktivní hodnocení nejsou k dispozici. Nejistoty v definicích zdůrazňují potřebu individuálních hodnocení, včetně progrese CKD, komorbidit a komplikací, stejně jako hodnocení nutričního stavu, což umocňuje potřebu multidisciplinárního vyšetření v této křehké populaci, nejlépe v souladu s konceptem personalizované medicíny.
Podvýživa související se souběžným chronickým onemocněním (DRM)
Podle terminologických pokynů ESPEN označuje pojem podvýživa související s dalším chronickým onemocněním „specifický typ podvýživy způsobený souběžnou nemocí“. Zánět je běžnou součástí akutních a chronických onemocnění, a je proto klíčovým faktorem ke vzniku svalového katabolismu a anorexie.(13)
Koncept, že podvýživa nevzniká pouze z nutričních deficitů, ale může být způsobena také metabolickými poruchami a nedostatkem fyzické aktivity, je vyjádřen v termínu ztráta bílkovin a energie (PEW), což je definováno jako přítomnost nutričních a metabolických poruch při úbytku tělesných zásob bílkovin a energie (tj. svalové a tukové hmoty).(13) DRM a PEW se do značné míry překrývají při identifikaci věkových a s nemocí souvisejících nutričních poruch.
Až donedávna nedostatek celosvětového konsenzu ohledně diagnostických kritérií pro podvýživu spolu s potřebou složitých a časově náročných hodnocení přispíval k omezení rutinní implementace výživové péče.(14) Globální iniciativa pro vedení v oblasti podvýživy (GLIM) nedávno vydala konsenzuální návrh na diagnostiku nemocí souvisejících s podvýživou založený na kombinovaných fenotypových a etiologických kritériích, s cílem poskytnout jednoduchý nástroj, který by byl použitelný v rutinní klinické praxi.(15) GLIM fenotypová kritéria zahrnují nízký index tělesné hmotnosti (BMI), úbytek hmotnosti a nízkou svalovou hmotu, zatímco etiologická kritéria zahrnují nechtěně nízký příjem potravy a přítomnost onemocnění a/nebo zánětu. GLIM kritéria se již používají v různých kombinacích v různých hodnoticích postupech.(16)
V tabulce 1 jsou uvedena kritéria pro diagnózu podvýživy podle GLIM a PEW. Pro diagnózu podvýživy podle kritérií GLIM je potřeba alespoň jedno fenotypové a jedno etiologické kritérium,(15) které by mělo být následováno kompletním nutričním hodnocením; pro diagnózu PEW je potřeba alespoň jedno kritérium ze tří ze čtyř domén.
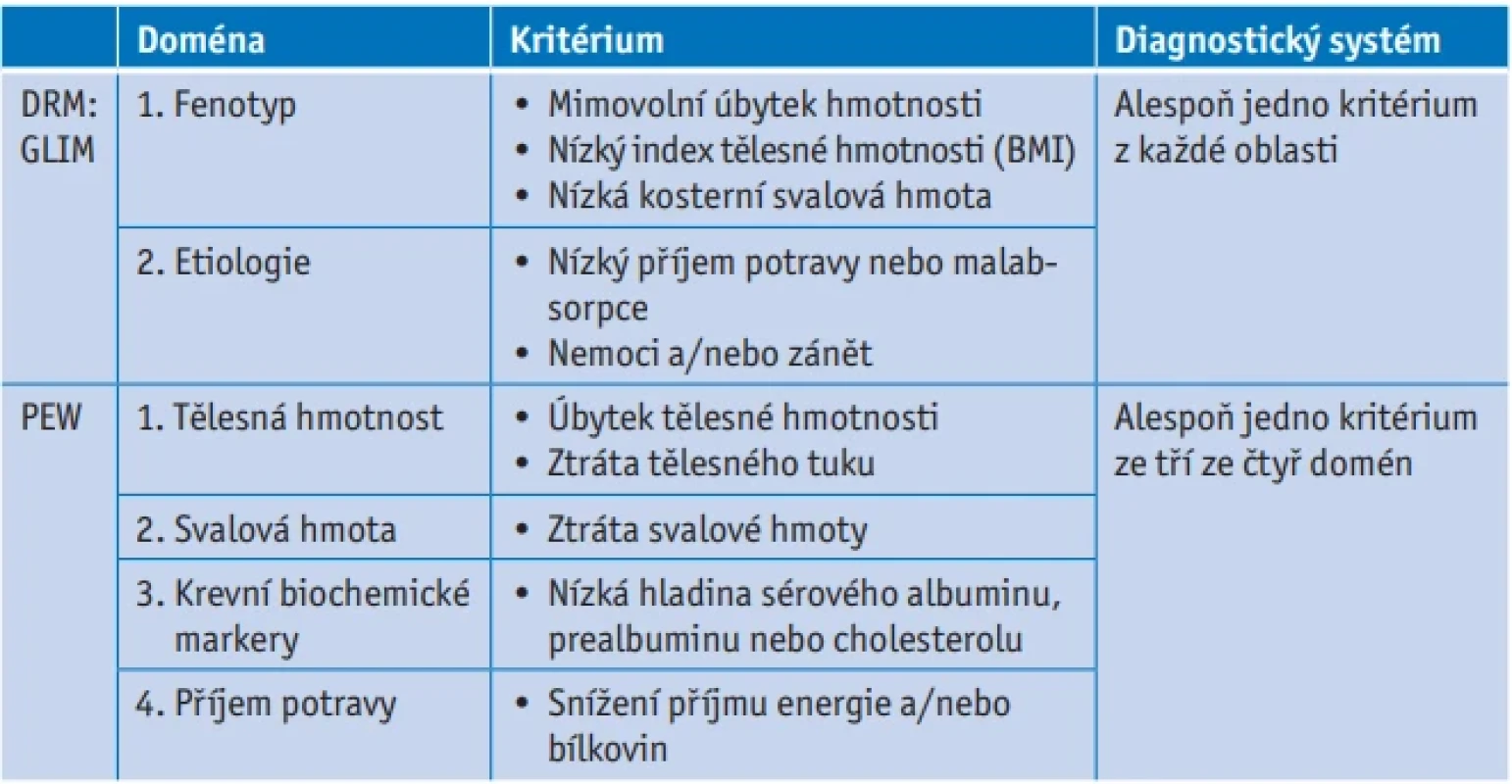
Důležité je, že zaměřením na nízkou svalovou hmotu obě kritéria také umožňují diagnózu DRM nebo PEW za přítomnosti obezity, což naznačuje, že je třeba věnovat zvláštní pozornost selektivním poruchám metabolismu (a příjmu bílkovin), a to i v přítomnosti zachovaných zásob tělesného tuku. To nutně souvisí s větší pozorností k životnímu stylu a cvičení jako prostředku ke zlepšení svalového metabolismu.(16, 17)
Je významné, že ačkoli diagnostika DRM nebo PEW nevyžaduje posouzení funkce kosterních svalů, nedávné pokyny KDOQI pro nutriční management CKD, v souladu s konsorciem GLIM, zdůrazňují důležitost pravidelného hodnocení funkce svalů jako součásti následného komplexního nutričního hodnocení a identifikují např. test úchopu jako praktický a snadno použitelný nástroj.(4, 6, 7)
V dostupných studiích u pacientů s CKD mají kritéria PEW i GLIM dobrou prediktivní hodnotu pro klinické výsledky a byla hlášena průměrná až velmi dobrá shoda mezi GLIM a PEW.(15, 17) ESPEN a ERA však uznávají, že rozdíly v rutinní terminologii mohou být matoucí, a podporují iniciativy zaměřené na definování společného jazyka, protože každá definice se může zaměřovat na různé aspekty stejného onemocnění, v souladu s jemnými nuancemi nutričního narušení.
Nutriční stav, riziko podvýživy a sarkopenie u seniorů s chronickým onemocněním
Definice „normálnosti“ ve vztahu ke věku je obtížná: proces stárnutí nevyhnutelně doprovází úbytek svalové hmoty a funkce, široce definované jako sarkopenie, ačkoli jeho rozsah a funkční dopad jsou vysoce heterogenní.(18) V důsledku toho je potřeba individuální analýza změn tělesné hmotnosti a složení těla v čase, aby se určilo, které nutriční intervence by byly pro konkrétního pacienta nejúčinnější.(19) Longitudinální studie u starších dospělých ukazují průměrný roční pokles svalové plochy přibližně o 5 % za každých 5 let a vyšší pokles svalové síly. Za ztrátou svalové hmoty stojí více vzájemně propojených faktorů. Kromě věkem podmíněného zhoršení příjmu energie a bílkovin a menší fyzické aktivity mohou s věkem často spojené metabolické poruchy urychlit katabolismus svalových proteinů a syntetickou reakci na anabolické podněty, což je stav nazývaný anabolická rezistence. Mitochondriální dysfunkce a postupné snižování počtu a velikosti svalových vláken typu II byly také popsány jako součást procesu stárnutí. Tyto změny mohou vést k dalším poruchám anabolismu svalových proteinů v přítomnosti metabolického stresu, například u akutních a chronických onemocnění.(20, 21) Ačkoli změny svalové hmoty nejsou vždy spojeny se změněnou funkcí svalů, variabilní ztráta svalové funkce je obvykle spojena s nízkou svalovou hmotou.
Paralelně se svalovými poruchami stárnutí vyvolává i absolutní nebo relativní nárůst tělesného tuku; hromadění především viscerálního tuku je často spojeno s poruchou metabolismu tuku, s hypertrofií adipocytů a prozánětlivými vzorci sekrece adipokinů a cytokinů, což přispívá k viscerální adipozitě zahrnující také svalovou tkáň.(21) Starší lidé často trpí nadváhou, proto by se měla přehodnotit i definice ideální tělesné hmotnosti pro tuto populaci. Mírný chronický zánět spojený s dysfunkční tukovou tkání a související inzulinovou rezistencí může urychlit svalový katabolismus a jeho funkční i klinické komplikace. GLIM kritéria, která berou v úvahu věkem podmíněné změny v tělesném složení, naznačují vyšší práh BMI pro diagnózu podvýživy u jedinců starších 70 let (22 kg/m2 ve srovnání s 20 kg/m2). Jak bylo zmíněno, splnění kritéria nízké kosterní svalové hmoty v GLIM a PEW umožňuje diagnostiku podvýživy i při normálním nebo vysokém BMI.(15)
Stále častěji uznávaný problém sarkopenie u osob s nadváhou nebo obezitou vedl k označení „sarkopenická obezita“, což zdůrazňuje redukci svalové hmoty u obézních osob; výskyt tohoto onemocnění se zvyšuje při stárnutí a u chronických onemocnění a je velmi častý ve stadiích CKD 3–5.(22)
Riziko malnutrice u seniorů s CKD
CKD je nejčastější příčinou DRM a PEW, a u seniorů je velmi často riziko malnutrice synergické. Navíc CKD u seniorů je často způsobeno významnými kardiometabolickými komorbiditami, jako je diabetes či kardiovaskulární onemocnění s obezitou, nebo je s nimi spojeno. Pro pacienty s CKD jsou malnutrice a PEW, zvláště spolu s úbytkem svalové hmoty, velmi významným prognostickým faktorem morbidity i mortality.(23) Spojení se syndromem MIA (malnutrice, zánět, ateroskleróza) zásadně ovlivňuje prognózu pacientů s CKD a na základě hodnocení SGA (subjective global assessment) a malnutričního-inflamačního skóre (MIS) lze i predikovat prognostická kritéria mortality, morbidity a progrese CKD.(24) K hodnocení lze využít i malnutričně-prozánětlivé parametry, jako je cholesterol a albumin (obojí snížené), i když u seniorů je více prediktivní albumin či transferin.(7) Je třeba zmínit, že tzv. spontánně nízký příjem bílkovin ve vyšším věku není vždy zjištěn a může být relativně méně častý, než se dříve předpokládalo, i u „velmi starých“ pacientů.
Obecně platí, že vedle spontánního neúmyslného snížení příjmu energie a hyperkatabolismu hrají významnou roli při vzniku podvýživy (PEW u CKD) u seniorů metabolické komorbidity a kardiovaskulární onemocnění.(13, 25) Zdůrazňuje se tak nutnost zvýšené opatrnosti při omezování příjmu bílkovin u křehkých pacientů s chronickým onemocněním ledvin, včetně zvýšení rizika, že eventuální dialýza bude špatně tolerována a bude spojena se zvýšenou morbiditou i mortalitou.(26, 27)
Diety se sníženým obsahem bílkovin pro pacienty s CKD
Nízký příjem bílkovin u CKD: možné přínosy a nevýhody
Nízkobílkovinné diety (s dostatečným příjmem energie) jsou základem nutriční léčby CKD ve všech věkových kategoriích, a to s kontrolou složení živin a redukcí nadměrného příjmu sodíku, draslíku a fosfátů.(7, 28) Řada studií i dlouholeté klinické závěry vedly ke snížení příjmu bílkovin v dietě, přičemž hlavním patofyziologickým důvodem – vedle důvodů metabolických – je snížení glomerulární hyperfiltrace v reziduálních nefronech.(28) Orální proteinové zátěže přispívají k hyperfiltraci se zvýšeným hemodynamickým stresem, zvýšenou produkcí cytokinů a růstových faktorů, nižší permselektivitou glomerulární membrány a zvýšeným tonem aferentní arterioly při zvýšených hladinách glukagonu.(1) Hyperfiltrace v nefronu zvyšuje intraglomerulární tlak a proteinurii, což vede ke glomeruloskleróze a tubulointersticiální fibróze, a tedy k progresi CKD. Tubulointersticiální fibróza je dále zesílena metabolickou acidózou, která je rovněž spojena s vysokým příjmem bílkovin, převážně živočišného původu.(29) Hladiny močoviny v séru úzce odrážejí příjem bílkovin a hyperazotemie zvyšuje karbamylaci bílkovin a tvorbu reaktivních kyslíkových látek. Acidóza, vysoká hladina močoviny a fosfátů také zvyšuje výskyt uremických toxinů produkovaných střevní mikrobiotou (například indoxyl sulfát, p-kresyl sulfát a trimethylamin N-oxid), což může snižovat chuť k jídlu a vést k začarovanému kruhu anorexie, metabolickým poruchám a hyperkatabolismu, který charakterizuje pokročilou formu CKD.(29, 30) Předepisování nízkobílkovinné diety má za cíl zpomalit pokles funkce ledvin, zmírnit metabolické poruchy způsobené ztrátou jejich metabolické funkce, a tím oddálit terminální selhání.(7, 12, 28, 30)
Je třeba poznamenat, že pokud nemá pacient CKD se sníženou funkcí, nelze automaticky spojit spontánní nízký příjem bílkovin s lepší funkcí ledvin (nižší příjem bílkovin může být spojen se stravovacími návyky nebo odrážet podvýživu související s onemocněním). Naopak vysoký příjem bílkovin je z hlediska progrese renálního onemocnění spojen s negativními dlouhodobými výsledky.(31–33) Nejdůležitější je, že dodržování nízkobílkovinných diet je zásadní pro jejich účinnost. Studie MDRD (Modifikace diety u onemocnění ledvin), první velká randomizovaná studie testující vliv nízkobílkovinných diet na onemocnění ledvin, prokázala v dlouhodobém horizontu významnou klinickou výhodu u pacientů na dietě.(34) Tento nález obecně zdůraznil důležitost dlouhodobého dodržování modifikované stravy.(35) Výsledky pozdějších studií o pozitivních účincích nízkobílkovinných diet u pokročilé CKD byly skutečně spojeny s přísným výběrem a pečlivým sledováním zapsaných pacientů.(36–39)
Diskuse spojené s obecnou implementací restrikce proteinů u pacientů s CKD souvisejí často s výběrem pacientů a přesností jejich sledování. Ačkoliv nevylučují starší pacienty, mají velké klinické studie, jejichž data jsou zahrnuta v metaanalýzách a doporučeních, tendenci omezovat nábor křehkých jedinců, a proto mohou poskytovat suboptimální informace o možných vedlejších účincích, včetně dopadu na nutriční stav a kvalitu života.(33, 35)
Zda nízkobílkovinné diety někdy zvyšují riziko podvýživy a PEW u nevybraných křehkých starších pacientů s chronickou chorobou ledvin, nelze tedy jednoznačně odvodit, protože výběrová kritéria obvykle zahrnují pacienty s nižším rizikem podvýživy. Velké observační studie nás také ujišťují o nutriční bezpečnosti diet s nízkým a velmi nízkým obsahem bílkovin, alespoň krátkodobě, pokud je zapojen zkušený personál, který monitoruje, radí a podporuje dodržování diet pacienty.(36–39) Tyto poznatky naznačují, že stravovací přístupy u onemocnění ledvin by měly být považovány za příklad přesné nutriční medicíny a přizpůsobeny každému pacientovi individuálně.(40)
Dopad nízkobílkovinných diet na kvalitu života starších dospělých s CKD, která může být již CKD ohroženy, je také dosud málo prozkoumán. Ačkoli existují omezené důkazy ve prospěch zlepšení kvality života, neexistují žádné důkazy o možném poškození způsobeném omezením příjmu bílkovin.(41–43) Je však třeba poznamenat, že tyto studie byly prováděny v prostředích, kde bylo nabízeno více možností stravování, a v kontextu vysoce personalizovaného nutričního přístupu. Za zmínku stojí, že nedávno byl zaznamenán zájem o testování nových dietních přístupů u skupiny starších dospělých s nízkou úrovní vzdělání.(44)
Dietní strategie: výběr z alternativ jídelních sestav u starších pacientů s CKD při dietách s nízkým obsahem bílkovin
Jedním z možných problémů, které mohou omezit dlouhodobé dodržování nízkobílkovinných diet, je jejich monotónnost, jež může způsobit dva opačné problémy: postupné snižování příjmu potravy (energie a kalorií) vedoucí k podvýživě či zhoršující se podvýživě nebo nedodržování předepsané diety.(40) Dietologové a nutriční terapeutky mohou významně pomoci dodržovat dietu tím, že navrhují personalizovaná, na míru šitá řešení; vhodné dietní sestavy lze také nalézt v kuchařkách a brožurách, ale dlouhodobý úspěch zřejmě vyžaduje intenzivní podporu,pravidelnou kontrolu a monitoring, jehož organizace (včetně vzdáleného monitorování a e-learningových programů) závisí na lokálních možnostech a stravovacích návycích.(1, 39)
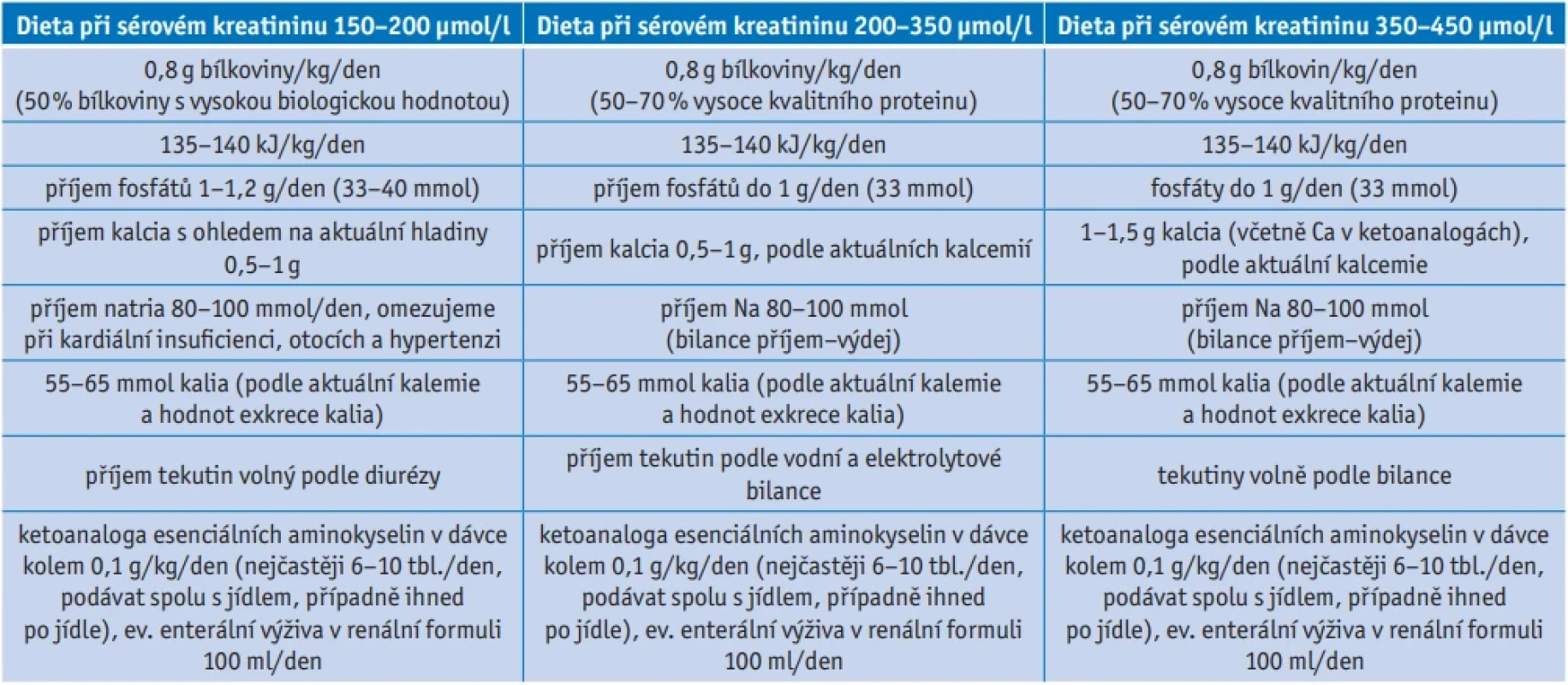
Existují různé možnosti nízkobílkovinných diet, přizpůsobené individuálním potřebám a preferencím, přičemž příklady jsou uvedeny v tabulce 2.(9,40–48)

Doporučené složení diet vychází z výsledků dlouhodobé klinické praxe podpořené daty prospektivní randomizované, dvojitě slepé, placebem kontrolované multicentrické studie CEKAD (Central European Keto Amino Acid Diet), kde bylo po dobu tří let sledováno celkem 300 nemocných ve stadiu CKD 3b–4, diabetiků i nediabetiků, z čehož 100 nemocných bylo z ČR.12
Specifika metodiky dietního programu u seniorů a nutriční opatření podle našich zkušeností
Při špatné compliance lze užít u seniorů modifikovaný příjem proteinů v dietě. Někteří autoři doporučují vložit do sedmidenního cyklu nízkobílkovinné diety (NB) dva dny s vyšším obsahem bílkovin (až 1 g/kg TH/den). Podle našich zkušeností, s ohledem na dlouhodobý metabolický stav nemocných a jídelní stereotyp, vkládáme většinou 1× týdně jídelní sestavu obsahující 0,8 g B/kg TH/den. V ostatních případech dáváme raději přednost nutričnímu suplementu či při špatné compliance a adherenci k dietě přechodu na volnější kontrolovanou dietu s obsahem 0,8 g B/kg TH/den s omezeným obsahem fosfátů. V současné době populární vegetariánská dieta se do určité míry blíží původní italské, resp. i bramboro-vaječné dietě německé. Na základě vegetariánské diety lze výhodně sestavit jídelní lístek pro všechny formy nízkobílkovinných diet.(49, 50) Pro nižší obsah esenciálních aminokyselin v některých vegetariánských pokrmech však musí být tyto diety suplementovány.(12) U diety přísně vegetariánské však nestačí samotný přísun rostlinné bílkoviny pokrýt základní potřebu esenciálních aminokyselin a tyto musí být bezpodmínečně suplementovány.
Významným pokrokem bylo nahrazení plnohodnotných esenciálních aminokyselin jejich keto - a hydroxyanalogy (KA). Uskutečněné studie využily mechanismu reverzibilní transaminace vybraných esenciálních aminokyselin.(36, 39) Podávání bezdusíkatých „uhlíkových skeletů“ esenciálních aminokyselin ve formě jejich keto - a hydroxyanalog vedlo jak k výraznému snížení příjmu exogenního dusíku do organismu, tak k využití části dusíku retinované močoviny k aminaci těchto aminokyselin.
Formou ketoanalog byly podávány aminokyseliny leucin, isoleucin, valin, fenylalanin a methionin. Ostatní esenciální aminokyseliny byly podávány ve své L-formě (lysin, threonin a tryptofan), neboť jejich aminace v organismu byla metabolicky náročná a méně efektivní. V sestavě aminokyselin byly doplněny histidin a tyrosin. V našich podmínkách nebyly většinou prokázány snížené hladiny histidinu, ale jeho využitelnost vázne. Histidin významně zlepšuje dusíkovou bilanci a podílí se i na stabilizaci krevního obrazu. Zatímco minimální denní potřeba esenciálních aminokyselin pro zdravé osoby byla stanovena již před více než 50 lety, není otázka adekvátní úhrady esenciálních aminokyselin u nemocných v chronické renální insuficienci dodnes zcela vyřešena.
U nás dostupné přípravky mají ketoanaloga vázána ve formě kalciových solí, což znamená při obsahu například 50 mg kalcia v 1 tbl. přípravku dostupných ketoanalog v ČR (Kemarel či Ketosteril) nezanedbatelný přísun kalcia.
Na úspěšnosti NB diet se nepochybně podílí dlouhodobě vyrovnaná metabolická bilance nemocných, účinná léčba hypertenze a pravidelné kontroly konané v této fázi onemocnění lékařem nejméně jedenkrát měsíčně. Vedle základních laboratorních parametrů (kreatinin, urea, glomerulární filtrace, KO, sideremie, ev. při léčbě rh-EPO feritin či saturace transferinu, Na, K, Ca, P, kyselina močová, Astrup, glykemie, cholesterol, triacylglyceroly, močový sediment, bakteriurie, proteinurie/24 hodin) musíme pravidelně kontrolovat základní parametry nutrice, tj. albumin, transferin, event. aminogram (resp. Whiteheadův kvocient, tj. poměr neesenciálních aminokyselin gly + glu + ser + tau a esenciálních aminokyselin leu + ileu + val + met). K základním údajům patří subjektivní pocity nemocného a jeho celková prosperita měřená antropometricky. Vedle tzv. adherence k dietě, kterou můžeme zhodnotit anamnesticky či lépe formou dotazníku, hodnotíme při nízkobílkovinné dietě tzv. compliance podle odpadu urey a fosfátů do moči za 24 hodin.
Funkce ledvin, metabolismus bílkovin a aminokyselin
Poznatek o existenci poruchy metabolismu bílkovin u nemocných s chronickým selháním ledvin má dlouholetou historii.(49, 50) V souladu s historickou tezí Giordana lze predikovat: Pokud organismus dostává denně dostatečné množství esenciálních aminokyselin, stává se limitujícím faktorem pro udržení dusíkové rovnováhy dusík pocházející z neesenciálních aminokyselin. Za těchto podmínek může být využit ke stavbě bílkovin i dusík pocházející z močoviny. Utilizace dusíku urey u nemocných v chronické renální insuficienci může být relativně vysoká (30–40 %). Lepší využití aminokyselin při nedostatečném příjmu bílkovin je umožněno zvýšenou aktivitou proteosyntetických enzymů v játrech, snížením jejich oxidace a snížením aktivity enzymů ureového cyklu. Pro přepočet vyloučeného množství urey v moči na příjem bílkovin či aminokyselin je nutno vědět, že z 1 g bílkovin vzniká přibližně 5,5 mmol urey a 80 % vytvořené urey se vylučuje močí. K prakticky snadno dosažitelným indikátorům intenzity proteinového metabolismu patří výpočet množství metabolizovaného (a za předpokladu vyrovnané metabolické bilance i přijatého) proteinu na podkladě množství urey vyloučené do moči v mmol za 24 hodin: (Uurea.V) × 0,25 (za předpokladu, že se fekálně vylučuje u těchto nemocných kolem 0,031 g N/kg/den). Spektrum aminokyselin v séru se při renální insuficienci zásadně mění. Snižují se koncentrace esenciálních aminokyselin (EAK) s výjimkou fenylalaninu. Koncentrace neesenciálních aminokyselin (NEAK) se většinou naopak zvyšuje. Snižuje se také poměr EAK : NEAK. Toto snížení je však výrazně ovlivňováno stavem nutrice. Vylučování aminokyselin do moči se při renální insuficienci podstatně nemění, což je způsobeno – při snížené glomerulární filtraci – zvýšenou frakční exkrecí aminokyselin.(12) Koncentrace aminokyselin v séru závisí na jejich intracelulárním metabolismu. Koncentrace volných aminokyselin je v intracelulární tekutině podstatně vyšší, než je v tekutině extracelulární. Tyto aminokyseliny pak mohou být transportovány do extracelulárního prostoru (např. při poklesu sérových hladin aminokyselin při ztrátách vyvolaných hemodialýzou.). Snížené hladiny rozvětvených esenciálních aminokyselin jsou jedním z typických nálezů u nemocných v chronické renální insuficienci. Také hladina serinu může být významně snížena, neboť ledviny jsou hlavním místem jeho tvorby. Mohou být ovlivněny hladiny dalších hydroxyaminokyselin (glycin a threonin). Hladina alaninu a glutaminu bývá většinou normální a tyto aminokyseliny představují v postdigesční fázi hlavní zdroj dusíku pro ledviny a splanchnické orgány. Jejich hladina je výrazně ovlivňována dietou, stejně jako stupněm vychytávání (metabolizace) v uvedených orgánech. Stejně tak se zvyšují hladiny některých aminokyselin ureového cyklu (především citrulinu, zatímco arginin zůstává většinou normální), aminokyselin obsahujících síru (cystinu, homocysteinu, event. cysteinu, zatímco hladina methioninu zůstává normální), prolinu, hydroxyprolinu a 3-metylhistidinu.
Pro malnutrici je typický pokles tělesné hmotnosti, tělesného tuku, svalové hmoty a intracelulární vody. Klesají hladiny albuminu, transferinu, cholinesterázy, komponent komplementového systému, především C3 složky. Stejně se snižují hladiny valinu, leucinu, isoleucinu, tryptofanu a tyrosinu, poměr celkových esenciálních aminokyselin k neesenciálním, valinu ke glycinu a tyrosinu k fenylalaninu, hladina glycinu je často zvýšena.(49) Tryptofan je jediná aminokyselina vázaná na bílkoviny séra a je mimořádně významná z hlediska zahájení proteosyntézy. Koncentrace tryptofanu v séru při CKD bývá normální nebo lehce snížená. Mění se však poměr volného a vázaného tryptofanu. Koncentrace vázaného tryptofanu se snižuje, zvyšuje se koncentrace volného tryptofanu. Tryptofan je zdrojem indolových látek, jejichž koncentrace se v renální insuficienci zvyšuje. Porucha metabolismu fenylalaninu a tyrosinu je známá již delší dobu. Uvádí se, že zvýšená hladina fenylalaninu, jeho zpomalená metabolizace a snížený poměr tyrosinu k fenylalaninu mohou být způsobeny jak snížením hladiny ledvinné fenylalaninhydroxylázy, tak změnou intra - a extracelulární distribuce. Je známou skutečností, že histidin je esenciální aminokyselinou pro nemocné v chronické renální insuficienci. Jeho plazmatické koncentrace bývají nízké, buď pro sníženou syntézu jeho prekurzoru (kyseliny imidazolpyrohroznové), nebo sníženou schopnost transaminovat tuto ketokyselinu (snížená aktivita transketolázy v chronické renální insuficienci).
Závažný příspěvek do hodnocení metabolického stavu nemocných v chronické renální insuficienci přinesly studie zabývající se intracelulární koncentrací aminokyselin, především ve svalové hmotě. Jak známo, kosterní svaly představují hlavní zásobní zdroj volných aminokyselin. V chronické renální insuficienci se mění extra/intracelulární distribuce některých aminokyselin, takže plazmatické hladiny nejsou odpovídajícím odrazem hladin intracelulárních. Tato skutečnost se například týká pro metabolismus velice důležitých tzv. rozvětvených aminokyselin, leucinu, isoleucinu a valinu. Při snížené plazmatické hladině těchto tří aminokyselin byly popsány normální intracelulární koncentrace leucinu a isoleucinu (valin byl snížen) a tyto rozdíly přetrvávaly i při dlouhodobé nízkobílkovinné dietě doplněné esenciálními aminokyselinami. Selektivní deplece valinu, a to přes vysoký příjem, ukazovala, že tato aminokyselina byla zvýšeně katabolizována a při uvedené suplementaci esenciálních aminokyselin vznikl mezi valinem a leucinem s isoleucinem tzv. aminokyselinový antagonismus. Podobně byla zjištěna výrazně snížená intracelulární hladina tyrosinu při relativně zvýšené hladině plazmatické. Threonin byl nalezen snížený jak v plazmě, tak ve svalu. Naproti tomu aminokyseliny ureového cyklu, citrulin, ornitin a arginin, byly nalezeny zvýšené jak ve svalu, tak v séru.(49, 50)
Je tedy zřejmé, že syntéza bílkovin v chronické renální insuficienci může být výrazně limitována intracelulárním obsahem aminokyselin, především pak nízkou koncentrací valinu, threoninu a tyrosinu a u neléčených též histidinu.
Optimalizace nutričních postupů u seniorů s chronickým onemocněním ledvin
Ačkoliv je hlavním tématem tohoto článku otázka příjmu bílkovin, je naprosto nutné zajistit a udržovat dostatečný příjem energie nezbytný pro využití bílkovin, a tím udržení optimálního klinického a nutričního stavu.(6, 7) Příjem energie nesmí klesnout pod bezpečnostní práh 20–25 kcal na kg denně (× 4,16 kJ, tj. 83,2–104 kJ). Individuální zhodnocení nutričního stavu by mělo zaručit adekvátní využití limitovaného příjmu živin.
Doporučení ESPEN pro výživu u geriatrických pacientů doporučují příjem energie 30 kcal/kg/den (124 kJ), ideálně optimalizovaný podle klidového energetického výdaje (REE). REE může s věkem klesat, především v důsledku poklesu beztukové a svalové hmoty, a může se i výrazně lišit u jednotlivce na základě biologické heterogenity, fyzické aktivity a komorbidit, přičemž bazální hodnoty jsou přibližně 20 kcal/kg/den.(6) Úpravy příjmu energie by měly být také založeny na stadiu renálního onemocnění, pohlaví a nutričním stavu (včetně obezity). V tomto kontextu směrnice KDOQI snížily předchozí indikaci minimální hodnoty 30–35 kcal/kg ideální tělesné hmotnosti za den na 25–30 kcal/kg/den u pacientů s chronickým onemocněním ledvin.(7)
Perorální výživové doplňky
Ketoanaloga
Pokud je příjem energie ve stravě považován za nedostatečný a nejsou dosaženy nutriční cíle, mohou být potřeba perorální výživové doplňky.(50) Krátkodobé zvýšení příjmu bílkovin (např. při hospitalizaci z chirurgických důvodů či během zotavování z akutního onemocnění) nepůsobí negativně na dlouhodobou funkci ledvin, ale zvýšení příjmu bílkovin může zhoršit metabolickou acidózu, hyperfosfatemii a zvýšit hladinu močoviny (a dalších toxinů), čímž potenciálně naruší metabolickou homeostázu a zhorší chuť k jídlu.(8)
Ketoanaloga esenciálních aminokyselin a směs aminokyselin se běžně používají ve stravách s nízkým obsahem bílkovin a v některých rostlinných dietách s mírným omezením bílkovin.(12)
Velikost dávky ketoanalog a esenciálních aminokyselin je závislá na bílkovinném složení diety, hmotnosti nemocného a jeho nutričním stavu. Při neselektivní nízkobílkovinné dietě obsahující 0,6 g bílkovin/kg/den se udává dávka 0,1–0,2 g aminokyselin/kg/den. Minimální dávka nezbytná k udržení dusíkové rovnováhy při naší dietě činila 4,8 g/den (přípravek Ketosteril či Kemarel).
Celkový příjem bílkovin včetně aminokyselin nesmí dlouhodobě klesnout pod 0,7 g/kg TH/den.
Kontraindikace v podávání ketoanalog jsou hyperkalcemie, uremická gastrointestinální symptomatologie a těžká jaterní léze.
Enterální výživa
Pokud se nám nedaří dosáhnout deklarovaného složení diety – především z hlediska energetického – a dále v zátěžových katabolických situacích (interkurentní onemocnění, operace, zvýšená fyzická zátěž, váhová neprosperita nemocných), užíváme tzv. suplementy. Nejjednodušší je užití doplňkových výživných nápojů. Jejich energetický základ tvoří maltodextrin a jsou ochuceny sirupem a džusem. Kombinované suplementy používáme při závažnějších metabolických poruchách výživy a preventivně při zvýšené zátěži organismu ve formě sippingu, nejlépe v renální formuli s vyšším obsahem energie, ale definovaným příjmem bílkoviny mléčné provenience (např. Nutrego renal, Fresubin renal, Nutricomp renal, Resource renal, Fresenius Kabi renal apod.). Obsah minerálů, stopových prvků a vitaminů je upraven s ohledem na renální insuficienci.(51)
U některých nemocných se nedaří snížit hyperlipoproteinemii pouze upravenou dietou. V těchto případech přidáváme některé formy rostlinné vlákniny, respektive pektinu. Zásah vlákniny do metabolismu má komplexní charakter a vedle snížení resorpce tuku zlepšuje i sacharidovou toleranci. Nevýhodou je potřeba užít poměrně velké dávky (20–40 g), čímž se může nebezpečně zvýšit přísun kalia do organismu.
U indikovaných nemocných s intolerancí sippingu doplňujeme k ordinované dietě energetické doplňky ve formě prášku, který je přidán přímo do vybraných jídel (speciální polysacharid) či doplňujeme (fortifikujeme) touto formou potraviny po stránce optimálního složení proteinů (mléčný protein).
Klinický závěr a doporučení
Personalizovaná výživa a individuální hodnocení rizika a přínosu
Personalizovaná výživa (PN) byla nedávno popsána jako „obor, který využívá lidskou individualitu k řízení výživových strategií, jež vedou k prevenci, zvládají a léčí nemoci a optimalizují zdraví; jsou vymezené třemi synergickými prvky: věda a nová data v oblasti PN, odborné vzdělávání a školení v oblasti PN a poradenství a terapie v oblasti PN“.(9)
Nutriční léčba u seniorů s chronickým onemocněním ledvin by měla být předepsána společným hodnocením nefrologů, nutricionistů, nutričních terapeutek a pochopitelně i pacienta, který musí doporučenou dietu dlouhodobě dodržovat. Výživový předpis by měl zohledňovat místní potravinové zvyklosti, jejich dosažitelnost (včetně ceny), zdroje, stejně jako přání a životní styl osoby, které je léčba určena.
Prvním krokem v rozhodovacím procesu je identifikace dominantního problému: CKD a léčba u staršího dospělého či seniora versus nutrice u staršího pacienta či seniora s CKD.
Hlavní léčebné cíle zahrnují: (1) oddálení dialýzy nebo vyhnutí se dialýze, (2) udržení nebo zlepšení nutričního stavu, (3) udržení nebo zlepšení kvality života.
Druhým krokem v rozhodovacím procesu je stanovení parametrů, které pomohou zajistit poskytování kvalitní výživové péče:
Hodnocení tolerance léčby pacienty při pravidelných kontrolách: mělo by být jedním z hlavních měřítek toho, jak pacient s CKD prosperuje, jak se cítí. Mělo by zohledňovat příznaky, vliv stravy na kvalitu života, duševní zdraví a společenský život.
Nutriční stav a renální funkce: v kontextu doporučení shrnutých v hlavním textu by monitorování výživového stavu mělo pravidelně zahrnovat klinické vyšetření s měřením tělesné hmotnosti a krevní a močové vyšetření základních nutričně-metabolických parametrů a funkce ledvin.
prof. MUDr. Vladimír Teplan, DrSc.
Absolvoval Lékařskou fakultu Univerzity Karlovy v Praze. V letech 1997–2007 byl přednostou Kliniky nefrologie IKEM, v letech 2008–2015 jejím zástupcem. Jako Oberarzt vedl nefrologické oddělení na klinice v Dessau (Sasko-Anhaltsko). S profesorem O. Schückem založil v roce 1995 Subkatedru nefrologie IPVZ, kterou dlouhodobě vedl. Je profesorem vnitřního lékařství na Lékařské fakultě Ostravské univerzity. Jako konzultant pracuje na klinikách Codum, Iscare a Ambicare v Praze, kde se výzkumně věnuje problematice metabolismu a výživy při konzervativní léčbě chronického onemocnění ledvin. Je autorem či významným spoluautorem 19 monografií a 75 kapitol v monografiích v České republice i v zahraničí.
Zdroje
1. Teplan V, et al. Nefrologie vyššího věku. Praha: Mladá fronta; 2015. Edice Aesculap.
2. United States Renal Data System. USRDS Annual Data Report: epidemiology of kidney disease in the United States. Bethesda (MD): National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases; 2022.
3. Koppe L, Fouque D, Kalantar-Zadeh K. Kidney cachexia or protein-energy wasting in chronic kidney disease: facts and numbers. J Cachexia Sarcopenia Muscle 2019; 10 : 479–484.
4. Cederholm T, Barazzoni R, Austin P, et al. ESPEN guidelines on definitions and terminology of clinical nutrition. Clin Nutr 2017; 36 : 49–64.
5. Donini LM, Busetto L, Bischoff SC, et al. Definition and diagnostic criteria for sarcopenic obesity: ESPEN and EASO consensus statement. Obes Facts 2022; 15 : 321–335.
6. Volkert D, Beck AM, Cederholm T, et al. ESPEN guideline on clinical nutrition and hydration in geriatrics. Clin Nutr 2019; 38 : 10–47.
7. Ikizler TA, Burrowes JD, Byham-Gray JD, et al. KDOQI clinical practice guidelines for nutrition in CKD: 2020 update. Am J Kidney Dis 2020; 76(Suppl 1): S1–S107.
8. Fiaccadori E, Sabatino A, Barazzoni R, et al. ESPEN guideline on clinical nutrition in hospitalized patients with acute or chronic kidney disease. Clin Nutr 2021; 40 : 1644–1668.
9. Piccoli GB, Cederholm T, Avesani CM, et al. Nutritional status and the risk of malnutrition in older adults with chronic kidney disease – implication for low protein intake and nutritional care: a critical review endorsed by ERN-ERA and ESPEN. Clin Nutr 2023; 42(4): 443–457.
10. Teplan V, Topinková E. Konzervativní léčení seniorů s chronickým onemocněním ledvin ve stadiu CKD 3b a vyšším. Geriatr Gerontol 2017; 6(1): 16–22.
11. Druml W, Cano N, Fiaccadori E, Teplan V. Nutritional support in renal disease. In: Sobotka L, ed. Basics in clinical nutrition. 5th ed. Praha: Galen; 2019 : 422–435.
12. Teplan V. Suplementované restriktivní diety u nemocných vyššího věku s onemocněním ledvin. Vnitř Lék 2016; 62(Suppl 6): 88–96.
13. Oliveira EA, Zheng R, Carter CE, Mak RH. Cachexia/protein energy wasting syndrome in CKD: causation and treatment. Semin Dial 2019; 32 : 493–499.
14. MacLaughlin HL, Friedman AN, Ikizler TA. Nutrition in kidney disease: core curriculum 2022. Am J Kidney Dis 2022; 79 : 437–449.
15. Cederholm T, Jensen GL, Correia M, et al. GLIM criteria for the diagnosis of malnutrition – a consensus report from the global clinical nutrition community. Clin Nutr 2019; 38 : 1–9.
16. Karavetian M, Salhab N, Rizk R, Poulia KA. Malnutrition-inflammation score vs phase angle in the era of GLIM criteria: a cross-sectional study among hemodialysis patients in UAE. Nutrients 2019; 11.
17. Davenport A. Comparison of frailty, sarcopenia and protein energy wasting in a contemporary peritoneal dialysis cohort. Perit Dial Int 2022; 42 : 571–577.
18. Gungor O, Ulu S, Hasbal NB,
Anker SD, et al. Effects of hormonal changes on sarcopenia in chronic kidney disease: where are we now and what can we do? J Cachexia Sarcopenia Muscle 2021; 12 : 1380–1392.
19. Sabatino A, Cuppari L, Stenvinkel P, et al. Sarcopenia in chronic kidney disease: what have we learned so far? J Nephrol 2021; 34 : 1347–1372.
20. Roshanravan B, Gamboa J, Wilund K. Exercise and CKD: skeletal muscle dysfunction and practical application of exercise to prevent and treat physical impairments in CKD. Am J Kidney Dis 2017; 69 : 837–852.
21. Donini LM, Busetto L, Bischoff SC, et al. Definition and diagnostic criteria for sarcopenic obesity: ESPEN and EASO consensus statement. Clin Nutr 2022; 41 : 990–1000.
22. Barreto Silva MI, Picard K, Klein M. Sarcopenia and sarcopenic obesity in chronic kidney disease: update on prevalence, outcomes, risk factors and nutrition treatment. Curr Opin Clin Nutr Metab Care 2022; 25 : 371–377.
23. Androga L, Sharma D, Amodu A, Abramowitz MK. Sarcopenia, obesity, and mortality in US adults with and without chronic kidney disease. Kidney Int Rep 2017; 2 : 201–211.
24. Jagadeswaran D, Indhumathi E, Hemamalini AJ, et al. Inflammation and nutritional status assessment by malnutrition inflammation score and its outcome in pre-dialysis chronic kidney disease patients. Clin Nutr 2019; 38 : 341–347.
25. Hanna RM, Ghobry L, Wassef O, et al. A practical approach to nutrition, protein-energy wasting, sarcopenia, and cachexia in patients with chronic kidney disease. Blood Purif 2020; 49 : 202–211.
26. Verberne WR, van den Wittenboer ID, Voorend CGN, et al. Health-related quality of life and symptoms of conservative care versus dialysis in patients with end-stage kidney disease: a systematic review. Nephrol Dial Transplant 2021; 36 : 1418–1433.
27. Voorend CGN, van Oevelen M, Verberne WR, et al. Survival of patients who opt for dialysis versus conservative care: a systematic review and meta-analysis. Nephrol Dial Transplant 2022; 37 : 1529–1544.
28. Kalantar-Zadeh K, Fouque D. Nutritional management of chronic kidney disease. N Engl J Med 2018; 378 : 584–585.
29. Carrero JJ, Gonzalez-Ortiz A,
Avesani CM, et al. Plant-based diets to manage the risks and complications of chronic kidney disease. Nat Rev Nephrol 2020; 16 : 525–542.
30. Koppe L, Fouque D. The role for protein restriction in addition to renin-angiotensin-aldosterone system inhibitors in the management of CKD. Am J Kidney Dis 2019; 73 : 248–257.
31. Lee SW, Kim YS, Kim YH, et al. Dietary protein intake, protein energy wasting, and the progression of chronic kidney disease: analysis from the KNOW-CKD study. Nutrients 2019; 11.
32. Windahl K, Faxen Irving G, Almquist T, et al. Prevalence and risk of protein-energy wasting assessed by subjective global assessment in older adults with advanced chronic kidney disease: results from the EQUAL study. J Ren Nutr 2018; 28 : 165–174.
33. Krok-Schoen JL, Archdeacon Price A, et al. Low dietary protein intakes and associated dietary patterns and functional limitations in an aging population: a NHANES analysis. J Nutr Health Aging 2019; 23 : 338–347.
34. Bellizzi V, Signoriello S, Minutolo R, et al. No additional benefit of prescribing a very low-protein diet in patients with advanced chronic kidney disease under regular nephrology care: a pragmatic, randomized, controlled trial. Am J Clin Nutr 2022; 115 : 1404–1417.
35. Torreggiani M, Fois A, Moio MR, et al. Spontaneously low protein intake in elderly CKD patients: myth or reality? Analysis of baseline protein intake in a large cohort of patients with advanced CKD. Nutrients 2021; 13.
36. Garneata L, Stancu A, Dragomir D, et al. Ketoanalogue-supplemented vegetarian very low-protein diet and CKD progression. J Am Soc Nephrol 2016; 27 : 2164–
2176.
37. Bellizzi V, Chiodini P, Cupisti A, et al. Very low-protein diet plus ketoacids in chronic kidney disease and risk of death during end-stage renal disease: a historical cohort controlled study. Nephrol Dial Transplant 2015; 30 : 71–77.
38. Koppe L, Cassani de Oliveira M, Fouque D. Ketoacid analogues supplementation in chronic kidney disease and future perspectives. Nutrients 2019; 11 : 2071.
39. Teplan V. Ketoanaloga esenciálních aminokyselin v konzervativní léčbě chronického onemocnění ledvin (CKD) u seniorů vysoké věkové kategorie (80–95 let). Aktual Nefrol 2023; 29(1): 6–17.
40. Ikizler TA. Very low-protein diets in advanced kidney disease: safe, effective, but not practical. Am J Clin Nutr 2022; 115 : 1266–1267.
41. Piccoli GB, Di Iorio BR, Chatrenet A, et al. Dietary satisfaction and quality of life in chronic kidney disease patients on low-protein diets: a multicentre study with long-term outcome data (Torino-Pisa study). Nephrol Dial Transplant 2020; 35 : 790–802.
42. Fois A, Torreggiani M, Trabace T, et al. Quality of life in CKD patients on low-protein diets in a multiple-choice diet system. Comparison between a French and an Italian experience. Nutrients 2021; 13.
43. Piccoli GB, Nazha M, Capizzi I, et al. Diet as a system: an observational study investigating a multi-choice system of moderately restricted low-protein diets. BMC Nephrol 2016; 17 : 197.
44. Longhitano E, Trabace T, Fois A, et al. Ready to change: attitudes of an elderly CKD stage 3–5 population towards testing protein-free food. Nutrients 2020; 12.
45. Cupisti A, Morelli E, Meola M, et al. Vegetarian diet alternated with conventional low-protein diet for patients with chronic renal failure. J Ren Nutr 2002; 12 : 32–
37.
46. Hamidianshirazi M, Shafiee M, Ekramzadeh M, et al Diet therapy along with nutrition education can improve renal function in people with stages 3–4 chronic kidney disease who do not have diabetes (a randomized controlled trial). Br J Nutr 2022; 128 : 1–
36.
47. Mocanu CA, Cuiban E, Paul Ret al. A supplemented very low-protein diet could be effective, safe, and feasible in closely monitored patients with advanced CKD. Am J Clin Nutr 2022; 116 : 836–837.
48. Teplan V, Petejová N, Valkovský I. Duální efekt ketoanalog esenciálních aminokyselin a inhibitorů SGLT2 receptorů u seniorů s chronickým onemocněním ledvin: tříleté klinické sledování. Vnitř Lék 2025; 71(7): 376–385.
49. Teplan V, Mengerová O. Dieta a nutriční opatření u chorob ledvin a močových cest. Praha: Mladá fronta; 2010. Edice Aesculap.
50. Teplan V, et al. Metabolismus a ledviny. Praha: Grada Publishing; 2000.
51. Teplan V. Klinická výživa u pacientů s onemocněním ledvin. In: Kohout P, ed. Klinická výživa. Praha: Galén; 2021 : 663–684.
Štítky
Geriatrie a gerontologie Praktické lékařství pro dospělé ProtetikaČlánek vyšel v časopise
Geriatrie a Gerontologie

2026 Číslo 1
-
Všechny články tohoto čísla
- Editorial
- Nutriční léčba a riziko podvýživy u seniorů s chronickým onemocněním ledvin – naše dlouholeté zkušenosti a algoritmus výživové péče dle ESPEN a ERN-ERA
- Iniciativa „Choosing Wisely“ v geriatrii: omezení nadbytečné „low-value“ péče
- Skupinové aktivity v přírodě jako dostupná a efektivní intervence podpory zdraví starších osob: implikace projektu RECETAS pro strategie zdravého stárnutí
- Proč nezapomínat na diferenciálně diagnostickou rozvahu osteoporózy ve stáří
- Specifika hypotyreózy v geriatrické populaci
- Integrovaná geriatrická péče o seniory s polymorbiditou s cílem podpory jejich funkčního stavu: projekt GeriPRO zahájen
- Informace SÚKL
- Hypolipidemická léčba u seniorů: mýtus, mezera nebo příležitost?
- Geriatrie a Gerontologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Hypolipidemická léčba u seniorů: mýtus, mezera nebo příležitost?
- Skupinové aktivity v přírodě jako dostupná a efektivní intervence podpory zdraví starších osob: implikace projektu RECETAS pro strategie zdravého stárnutí
- Integrovaná geriatrická péče o seniory s polymorbiditou s cílem podpory jejich funkčního stavu: projekt GeriPRO zahájen
- Proč nezapomínat na diferenciálně diagnostickou rozvahu osteoporózy ve stáří

